Stichwortsonntag
Atomaufbau
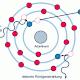
Ein Atom besteht aus einem Atomkern mit positiv geladenen Protonen und neutral geladenen Neutronen, sowie einer Atomhülle mit negativ geladenen Elektronen. Die Elektronen sind auf Schalen um den Atomkern aufgeteilt.
- Die Schalen nennt man von innen nach aussen: K, L, M, N, ...
- Man berechnet die höchstmögliche Anzahl von Elektronen auf einer Schale nach derFormel: 2n² . Das sind z.B. dann auf der innersten K-Schale zwei Elektronen und auf der nächst äußeren L- Schale acht Elektronen.
- Jede Schale bestrebt immer mit Elektronen voll besetzt zu sein. (Edelgaskonfiguration)

- Die Massenzahl [A] beschreibt die Anzahl der Protonen und Neutronen in einem Atom.
- Die Ordnungszahl [Z] beschreibt hingegen nur die Anzahl der Protonen im Kern.
- Atome mit gleicher Ordnungszahl, aber unterschiedlicher Massenzahl nennt man Isotope. Sie besitzen die gleiche Anzahl an Protonen aber eine unterschiedliche Anzahl von Neutronen.
- Ionen sind geladene Atome: Das heisst ,dass sie entweder mehr Protonen als Elektronen besitzen und somit positiv geladen wäre oder mehr Elektronen als Protonen besitzen und somit negativ geladen wären. Diese Konstellationen können zum Beispiel durch Röntgenstrahlen verursacht werden.
- Die Energie zwischen dem Kern und der Schale nennt man Bindungsenergie. Die Elektronen haben auf den verschiedenen Bahnen verschiedene Energiezustände. Umso weiter die Elektronen auf einer inneren Bahn liegen, umso höher ist ihre Bindungsenergie, aber der Energiezustand der Elektronen nimmt mit der Entfernung zu.
- Die Bindungsenergie ist also abhängig von der Entfernung zu den Schalen.
- Außerdem ist die Ordnungszahl für die Stärke der Bindungsenergie der einzelnen Elektronen verantwortlich. Umso höher die Ordnungszahl ist, desto stärker ist die Bindungsenergie des Einzelnen Elektrons.
- Diese Energie wird in ElektronenVolt, kurz eV gemessen. Diese Einheit bezeichnet die Energie, die ein geladenes Teilchen nach durchlaufen der Potentialdiffernz (Spannung) von 1 V in Vakuum als kinetische Energie gewonnen hat. Die kinetische Energie kann man auch Bewegungsenergie nennen und ist die Energie, die in der bewegten Masse eines Körpers enthalten ist.
- Eine Anregung eines Atoms entsteht, wenn eine genügend hohe Energie einem Atom hin zugeführt wird und ein gebundenes Elektron aus seiner Schale, also seinem Grundzustand heraus gelöst wird. Nun belegt das Elektron eine freie Position auf einer Kernfernen Schale, es verbleibt jedoch im Atomverbund.
- Bei einer Ionisation eines Atoms wird eine stärkere Energie zugeführt und ein Atom wird aus einem Grundzustand beziehungsweise aus seiner Schale heraus gelöst und verlässt den Atomverbund ganz. Er wird aus der Kernbindung heraus gelöst. Man unterscheidet zwischen der Stoßionisation bei der Elektronen durch andere energiereichere Elektronen aus Atomen oder Molekülen geschlagen und diese dadurch ionisiert werden und der Phtoionisation bei der die Atome oder Moleküle z. B. eines Gases durch kurzwellige Strahlung eines oder mehrerer ihrer Elektronen beraubt werden, spricht man von der Photoionisation.



Kommentieren